 Yemek
Yemek
 Yaşam
Yaşam
 Teknoloji
Teknoloji
 Seyahat
Seyahat
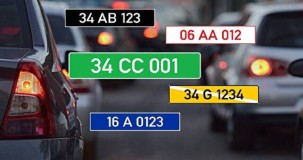 Otomobil
Otomobil
 Moda ve Güzellik
Moda ve Güzellik
 Kültür ve Sanat
Kültür ve Sanat
 Faydalı Bilgiler
Faydalı Bilgiler
 Eğitim
Eğitim
İyonik bağ , zıt yüklü iyonlar arasındaki elektrostatik kuvvetlere dayanan bir kimyasal bağ türüdür.
Oluşumu :
Özellikleri :
H2O molekülleri arasında hidrojen bağı bulunur.
HCl'de (hidrojen klorür) polar kovalent bağ bulunur. Kovalent bağ: HCl'de hidrojen (H) ve klor (Cl) atomları elektronları paylaşır. Polar bağ: Klorun elektronegatifliği (3,0) hidrojenin elektronegatifliğinden (2,1) daha büyük olduğu için ortaklaşa kullanılan elektronlar klor atomuna daha yakın olur ve HCl molekülü kutupsal bir molekül haline gelir.
Evet, metal iyonik bağ yapabilir. İyonik bağ, bir metal atomunun elektron vererek pozitif bir iyon (katyon) oluşturduğu ve bir ametal atomunun bu elektronu alarak negatif bir iyon (anyon) oluşturduğu durumlarda oluşur. Örneğin, sofra tuzu olarak bilinen sodyum klorür (NaCl) kristallerindeki sodyum ve klor atomları arasında iyonik bir bağ bulunur.
Kovalent ve iyonik bağ arasındaki temel farklar şunlardır: İyonik Bağ: Elektron transferi: Bir atom elektron verir, diğer atom elektron alır. Yük dengesizliği: Elektron transferi sonucu zıt yüklü iyonlar oluşur. Yüksek kaynama ve erime noktaları: Güçlü elektriksel bağlar nedeniyle. Elektrik iletkenliği: Katı halde elektrik iletkenliği yoktur, ancak çözeltide veya sıvı halde iyi iletken olur. Örnekler: Sodyum klorür (NaCl), magnezyum oksit (MgO). Kovalent Bağ: Elektron paylaşımı: Atomlar elektronları ortaklaşa kullanır. Düşük erime ve kaynama noktaları: Moleküller arasındaki bağlar genellikle daha zayıftır. Elektrik iletkenliği: Genellikle elektrik iletkenliği göstermez. Çözünürlük: Polar çözücülerde çözünür, apolar çözücülerde çözünmeyebilir. Örnekler: Su (H₂O), karbondioksit (CO₂), metan (CH₄).
Metalik ve iyonik bağlar arasındaki temel farklar şunlardır: Bağ Kurucular: İyonik bağlar, bir metal ve bir ametal arasında elektron alışverişi ile oluşurken, metalik bağlar iki metal arasında serbest elektronların hareketi ile oluşur. Elektronegatiflik: İyonik bağda atomlar arasındaki elektronegatiflik farkı belirgin iken, metalik bağda bu fark düşüktür. Bağın Gücü: Metalik bağ, serbest elektronlar ve pozitif iyonlar arasındaki elektrostatik çekim nedeniyle genellikle iyonik bağdan daha güçlüdür. Elektrik İletkenliği: İyonik bağlı katılar hareket etmediği için elektrik akımını iletmezken, metallerin serbest hareket edebilen değerlik elektronları sayesinde elektrik iletkenliği yüksektir. Kristal Yapı: İyonik bağlar genellikle kristal yapıdayken, metallerin katı halde kristal örgüsü bulunur.
İyon, bir veya daha fazla elektron kazanmış ya da yitirmiş bir atomdan (veya bir atom grubundan) oluşmuş elektrik yüklü parçacıktır. İyonlar, pozitif yüklü (katyon) ve negatif yüklü (anyon) olarak ikiye ayrılır. Katyon: Protonlardan daha az elektronu olan pozitif yüklü iyondur. Anyon: Protonlardan daha fazla elektronu olan negatif yüklü iyondur. İyonlar, doğal olarak atmosferde, şelalelerden dökülen su gibi hareket eden suların içinde veya yıldırım, yağmur ve bulutlardaki sürtünme gibi doğal olaylar sonucu oluşabilir.
Kovalent ve iyonik bağların gücü farklı faktörlere bağlıdır: Kovalent bağın gücü, paylaşılan elektron sayısına ve atomlar arasındaki çekim kuvvetine bağlıdır. İyonik bağın gücü ise şu faktörlere bağlıdır: İyon yarıçapı: İyon yarıçapı arttıkça iyonik bağın gücü azalır. İyon yükü: İyon yükü arttıkça çekim gücü artar ve iyonik bağın kuvveti artar. Kovalent bağlar, atomlar arasında elektron paylaşımına dayandığı için genellikle daha zayıftır.
 Eğitim
Eğitim
Yapay ve doğal seçilime örnek nedir?
İyonik bağ nedir?
XVI. yüzyıl kaçıncı yüzyıl oluyor?
Protistalar tek hücreli mi?
Çivi yazısını Anadolu'ya hangi uygarlık getirmiştir?
Safsata örnekleri nelerdir?
Sud kostik asit mi baz mı?
Rüzgarı Dizginleyen Çoçuk ne anlatıyor?
Selçuk edu öğrenci girişi nasıl yapılır?
Özlem Gürses hangi okul mezunu?
Vasco Da Gama neden önemli?
Ümitcan Hoca 7.sınıf ingilizce kaç kelime?
Okullarda pazar günü tatil mi?
Nikola tesla neden öldü ve cesedi neden kayboldu?
Piaget'e göre özümleme nedir?
Toprak hacim ağırlığı nasıl hesaplanır?
Son katmanında 8 elektron bulunmayan soy gaz nedir?
İnce ve kalın kenarlı mercek arasındaki fark nedir?
Proton sayısı nedir?
Sinüs ve kosinüs indirgeme nedir?
İkinci öğretim bölümleri nelerdir?
Protein sentezi nedir?
Çıraklık eğitim hangi bölümler var?
Uzman Öğretmenlik Sertifikası e-devletten nasıl görüntülenir?
Son 5 nüfus sayımı kaç yılda bir yapılır?
Süzern ve vassel ilişkisi nedir?
Özel eğitim bireysel gelişim raporu nereden alınır eğitimhane?
Soyağacında erkek ve dişi nasıl gösterilir?
Ve no3 ne anlatıyor?
Rizom ve kök arasındaki fark nedir?
ODTÜ Türkiye'de nerede bulunur?
Vertisol toprak nerede görülür?
Pürin nedir?
Volkmann kanallarında sadece toplardamar mı var?
Yeşil renk hangi renk olarak görülür?
Tam sayılı ve bileşik kesir hangisi daha büyük?
İyonosfere neden önemli?
Renklendirme yöntemi ile eğim nasıl bulunur?
Twitter'da öğretmen olmak için ne yapmalı?
Telegram Türk Paylaşım Grubu Nedir?